您的位置:首页 > 新闻中心 > 如何稀释溶液

如何稀释溶液
2024.10.31 点击2430次
溶液稀释是指通过加入溶剂,实现降低溶液浓度的过程。
一步稀释(稀释因子)法
根据所需浓度,将溶质与溶剂按适当的体积比例混合。例如,以1:n稀释化学品,表明每n份体积单位溶液中含有1份化学品和n-1份溶剂,该溶液稀释因子(DF, Dilution Factor)为n。
连续稀释法
逐步稀释,每一步待稀释溶液均来源于其前一步。例如,分两步将溶液以1:100稀释。
第一步:将原溶液以1:20稀释第二步:将第一步中溶液以1:5再稀释,得到最终稀释因子为100的溶液。
稀释方程法
其中,C1、 C2分别是初始、最终溶液浓度,V1 、V2分别是初始、最终溶液体积。将已知数据代入方程,即可得到所需信息。
摩尔浓度法
摩尔浓度(物质的量浓度)定义为溶液中溶质物质的量除以溶液(混合物)的体积,单位M=mol×L-1。采用如下公式可根据摩尔浓度稀释溶液:

百分比浓度法
溶液百分比浓度是指溶液所含溶质重量的百分比,单位%。比如,制备70%乙醇,需将70ml的100%乙醇和30ml的水混合。
值得注意的是,百分比浓度与摩尔浓度可以相互转换。
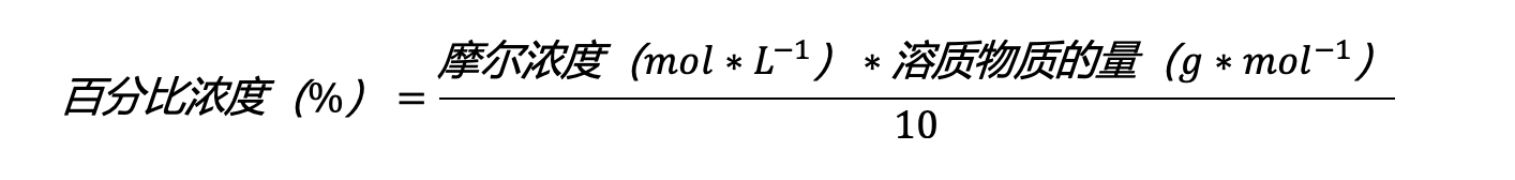
参考资料:
Mississippi State University. “Preparing Solutions and Making Dilutions”
J&K




